讲座预告:新冠急重症及转阴后遗症治疗医案一例 (讲座前作业)
男 成
病史
服用:麻黄升麻汤
麻黄6 升麻12 当归9 知母9 黄芩9 玉竹9 白芍9 天门冬12 桂枝9 茯苓9 炙甘草6 生石膏30 白术9 干姜9
嗓子剧痛,不能吞咽,咳嗽加剧,吐出很多白痰。
2022年1月29日-1月30日
持续发烧38.3由于白痰量多,改方:小青龙汤+石膏,体温不超过38,嗓子疼痛缓解,咳嗽开始带喘,无恶寒。
服后体温由38.5度降至37.4度,继续服用真武汤后,体温逐渐升至39度。
2022年2月3日
体温维持在38.6度。血氧仪测量血氧含量为91,心跳100/分钟。气喘明显。
服用乌梅丸
乌梅30 细辛6 桂枝9 黄连9 黄柏6 当归9 党参9 附子汤1包 花椒4 干姜9
情况没有太大改善,没有变好,也没有变坏。
2022年2月4日
服用桑菊饮
桑叶15 菊花9 杏仁6 桔梗9 连翘9 芦根30 炙甘草6 薄荷6
服用后,血氧含量提高到99,但是出现高烧39度。喘未减,夜晚无法入睡。
2022年2月5日
高烧39度,气喘,咳嗽,血氧含量86。


从2月6日开始,服用了正确药方,并找到家用制氧机,开始吸氧辅助治疗。情况逐渐好转,2月10日以后,体温完全正常并保持稳定。进入下一阶段治疗,新冠转阴后遗症治疗-----体位性心动过速综合征(POTS)以及肺脏功能血氧含量的康复。
————————————————————————————————————————————————————
经过第一阶段的治疗,体温均恢复正常,但心跳很快:
这种情况西医临床称为体位性心动过速,
请就文中给出资料在讲座前进行两个阶段的模拟看诊,并提交作业
附文西医对该疾病的认识:
前两期文章与大家分享了体位与血压和心律失常的关系,我们知道,卧位可以导致卧位型心绞痛和卧位性心律失常,直立位可以导致低血压或高血压,除此之外,直立位也可能导致心律失常。本期文章将与大家共同探讨和学习体位性心动过速综合征(POTS)。
探索历程
关于POTS的记载可追溯至1871年,当时将其称为“烦躁的心”(irritable heart)或“士兵的心”(soldier heart),用于形容战争中士兵出现异常的心动过速。直至1944年,才将其命名为“直立性心动过速”,特点是直立位时心率明显增加而血压仅有轻度下降,常伴有直立性心慌、轻度的头痛、乏力以及不能耐受运动。
20世纪80年代,随着倾斜试验的开展,越来越多的POTS病例被报道。1993年,Schondorf和Low提出了体位性心动过速综合征的概念,并用倾斜试验对患者进行评价,发现患者对倾斜试验的反应显著异常。在倾斜2分钟内心率很快升至120~170次/分,常伴肌肉震颤,部分患者的血压有轻度下降或舒张压升高。
随着POTS的研究不断深入,美国心律学会(HRS)于2015年首次发布了与自主神经系统相关的特殊性心律失常管理专家共识,以促进临床医生对POTS的认识。
临床特征
➤站立时常出现头晕、心悸、震颤、全身乏力、视野模糊等症状,不能耐受运动和疲劳
➤从卧位转为站立位时,心率加快≥30次/分(12~19岁:心率加快≥40次/分)并持续至少30秒
➤无直立性低血压(收缩压下降>20 mmHg)
发病机制
POTS是多种机制共同作用的结果,包括自主神经病变、低血容量、RAAS系统失调、中枢性肾上腺素能亢进、肥大细胞活化和自身免疫性等。
目前,关于POTS的发病机制的意见尚不统一,主要涉及如下几种:
(1)有研究发现部分患者存在下肢自主神经病变,下肢内因交感神经系统激活释放的去甲肾上腺素较正常人少。当患者在直立位时,因下肢自主神经功能失调,下肢静脉过度扩张、重力池作用增强,回心血量减少,继发性激活交感神经,使心率增快。另有学者认为是回心血量减少导致心肌缺血引起的心率增快。
(2)RAAS系统失调,研究发现部分患者血浆肾素活性、血管紧张素II和醛固酮水平未能在血容量减低时出现相应的升高,使得回心血量减少,进而导致心动过速。此外,还有很多不明原因所导致的原发性血容量减少引起POTS。
(3)中枢性肾上腺素能亢进,引起心率增快以及外周血管收缩、回心血量增多,导致心房、心室负担加重,使心肌的不应期和应激性发生改变,从而导致心动过速,这些患者可能有直立性高血压(收缩期血压升高>10 mmHg),并伴有震颤、焦虑和寒冷、四肢酸痛等症状。此外,去甲肾上腺素转运体(NET)基因的功能缺失也可引起肾上腺素能亢进。
此外,部分患者发生POTS可能是肥大细胞活化障碍,或是由于对疲劳和运动不耐受,导致心搏量减少和反射性心动过速,部分POTS也有免疫因素的参与,可能与神经节苷脂受体(NACHR)抗体或α1肾上腺素能受体抗体相关等。
诊断评估

治疗方案
目前针对POTS 尚缺乏有效的治疗措施,也尚无统一的具体治疗方法建议,通常需联合
几种治疗手段,建议多学科联合治疗。
结语
近年来,直立性不耐受的相关研究越来越多,但是对POTS发病机制的认识仍存在局限。正确识别、诊断POTS,对于不同类型的患者接受相应治疗极为关键,期待更多的研究结果来指导临床决策
。
男 成
病史
- 2022年1月27日
- 开始有微咳,发烧37.6度 ,轻度恶寒,轻度头痛,但无紧脉,舌像正常。
| 左外 | 左内 | 右内 | 右外 | |
| 整手脉 | 沉细弦滑数 | 沉细弦滑数 | ||
| 寸 | 沉弦 | 沉细弦滑 | 沉弦滑 | 沉弦 |
| 关 | 弱 | 沉弦滑 | 沉弦滑 | 滑 |
| 尺 | 弦 | 沉弦 | 弦 | 弦 |
服用:麻黄升麻汤
麻黄6 升麻12 当归9 知母9 黄芩9 玉竹9 白芍9 天门冬12 桂枝9 茯苓9 炙甘草6 生石膏30 白术9 干姜9
嗓子剧痛,不能吞咽,咳嗽加剧,吐出很多白痰。
2022年1月29日-1月30日
持续发烧38.3由于白痰量多,改方:小青龙汤+石膏,体温不超过38,嗓子疼痛缓解,咳嗽开始带喘,无恶寒。
- 2022年1月31日-2月2日
- 体温逐渐又回升至38.5度,有疲劳感,服用:真武汤
服后体温由38.5度降至37.4度,继续服用真武汤后,体温逐渐升至39度。
2022年2月3日
体温维持在38.6度。血氧仪测量血氧含量为91,心跳100/分钟。气喘明显。
服用乌梅丸
乌梅30 细辛6 桂枝9 黄连9 黄柏6 当归9 党参9 附子汤1包 花椒4 干姜9
情况没有太大改善,没有变好,也没有变坏。
2022年2月4日
服用桑菊饮
桑叶15 菊花9 杏仁6 桔梗9 连翘9 芦根30 炙甘草6 薄荷6
服用后,血氧含量提高到99,但是出现高烧39度。喘未减,夜晚无法入睡。
2022年2月5日
高烧39度,气喘,咳嗽,血氧含量86。
- 服用乌梅丸合桑菊饮,体温维持在38.6-39.5度之间。
- 去医院看急诊,做了理化检测和X光检查。
- 西医治疗:
- 输液:生理盐水、葡萄糖各500毫升。口服两粒Advil退烧。开了抗生素(未服用)。未留院治疗回家。
- 新冠检测阳性
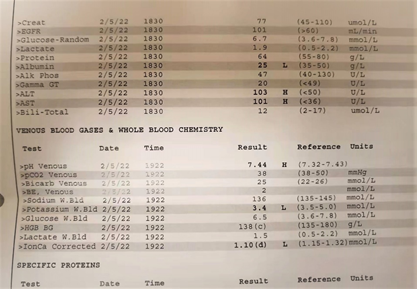
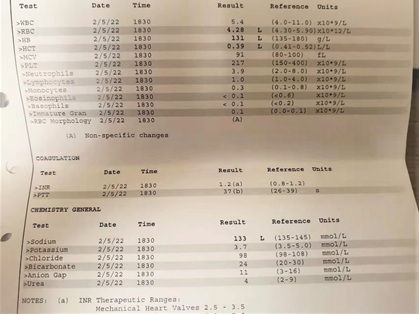
- 检测报告如下:
- 2022年2月6日晚,在家中
从2月6日开始,服用了正确药方,并找到家用制氧机,开始吸氧辅助治疗。情况逐渐好转,2月10日以后,体温完全正常并保持稳定。进入下一阶段治疗,新冠转阴后遗症治疗-----体位性心动过速综合征(POTS)以及肺脏功能血氧含量的康复。
————————————————————————————————————————————————————
经过第一阶段的治疗,体温均恢复正常,但心跳很快:
- 只要站立,心率即在100/分钟以上,经常是120/分钟,不敢走路,在平层慢走15米,血氧就掉到88;
- 吃饭后心跳在100-110/分钟;
- 夜晚睡眠时心跳68-72/分钟;
- 坐位90/分钟, 站立110-120/分钟,卧室慢走94-100/分钟。
这种情况西医临床称为体位性心动过速,
请就文中给出资料在讲座前进行两个阶段的模拟看诊,并提交作业
附文西医对该疾病的认识:
一文读懂:体位性心动过速综合征
医脉通 2018-04-27 王玉伟 金迪 潍坊市益都中心医院心血管内科 2347
前两期文章与大家分享了体位与血压和心律失常的关系,我们知道,卧位可以导致卧位型心绞痛和卧位性心律失常,直立位可以导致低血压或高血压,除此之外,直立位也可能导致心律失常。本期文章将与大家共同探讨和学习体位性心动过速综合征(POTS)。
探索历程
关于POTS的记载可追溯至1871年,当时将其称为“烦躁的心”(irritable heart)或“士兵的心”(soldier heart),用于形容战争中士兵出现异常的心动过速。直至1944年,才将其命名为“直立性心动过速”,特点是直立位时心率明显增加而血压仅有轻度下降,常伴有直立性心慌、轻度的头痛、乏力以及不能耐受运动。
20世纪80年代,随着倾斜试验的开展,越来越多的POTS病例被报道。1993年,Schondorf和Low提出了体位性心动过速综合征的概念,并用倾斜试验对患者进行评价,发现患者对倾斜试验的反应显著异常。在倾斜2分钟内心率很快升至120~170次/分,常伴肌肉震颤,部分患者的血压有轻度下降或舒张压升高。
随着POTS的研究不断深入,美国心律学会(HRS)于2015年首次发布了与自主神经系统相关的特殊性心律失常管理专家共识,以促进临床医生对POTS的认识。
临床特征
➤站立时常出现头晕、心悸、震颤、全身乏力、视野模糊等症状,不能耐受运动和疲劳
➤从卧位转为站立位时,心率加快≥30次/分(12~19岁:心率加快≥40次/分)并持续至少30秒
➤无直立性低血压(收缩压下降>20 mmHg)
发病机制
POTS是多种机制共同作用的结果,包括自主神经病变、低血容量、RAAS系统失调、中枢性肾上腺素能亢进、肥大细胞活化和自身免疫性等。
目前,关于POTS的发病机制的意见尚不统一,主要涉及如下几种:
(1)有研究发现部分患者存在下肢自主神经病变,下肢内因交感神经系统激活释放的去甲肾上腺素较正常人少。当患者在直立位时,因下肢自主神经功能失调,下肢静脉过度扩张、重力池作用增强,回心血量减少,继发性激活交感神经,使心率增快。另有学者认为是回心血量减少导致心肌缺血引起的心率增快。
(2)RAAS系统失调,研究发现部分患者血浆肾素活性、血管紧张素II和醛固酮水平未能在血容量减低时出现相应的升高,使得回心血量减少,进而导致心动过速。此外,还有很多不明原因所导致的原发性血容量减少引起POTS。
(3)中枢性肾上腺素能亢进,引起心率增快以及外周血管收缩、回心血量增多,导致心房、心室负担加重,使心肌的不应期和应激性发生改变,从而导致心动过速,这些患者可能有直立性高血压(收缩期血压升高>10 mmHg),并伴有震颤、焦虑和寒冷、四肢酸痛等症状。此外,去甲肾上腺素转运体(NET)基因的功能缺失也可引起肾上腺素能亢进。
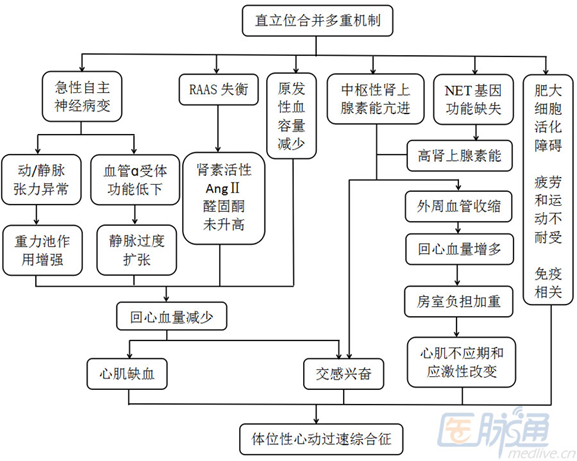
此外,部分患者发生POTS可能是肥大细胞活化障碍,或是由于对疲劳和运动不耐受,导致心搏量减少和反射性心动过速,部分POTS也有免疫因素的参与,可能与神经节苷脂受体(NACHR)抗体或α1肾上腺素能受体抗体相关等。
图1 体位性心动过速综合征的发病机制
诊断评估
表1 POTS 诊断评估方法
治疗方案
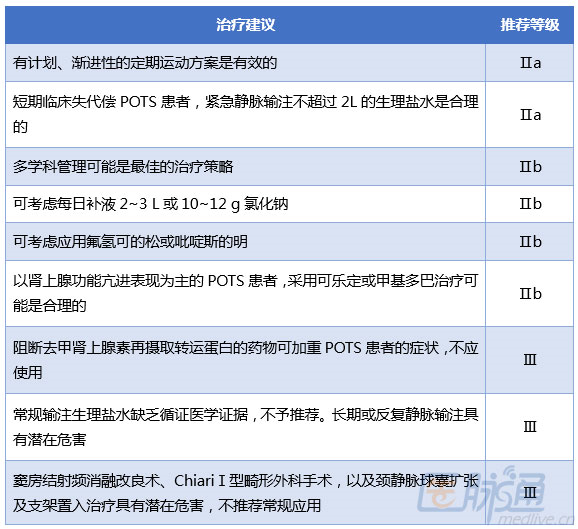
目前针对POTS 尚缺乏有效的治疗措施,也尚无统一的具体治疗方法建议,通常需联合
几种治疗手段,建议多学科联合治疗。
表2 POTS 的治疗建议
结语
近年来,直立性不耐受的相关研究越来越多,但是对POTS发病机制的认识仍存在局限。正确识别、诊断POTS,对于不同类型的患者接受相应治疗极为关键,期待更多的研究结果来指导临床决策
。


